Ostra białaczka szpikowa to nowotwór krwi i szpiku, który potrafi rozwinąć się w ciągu kilku tygodni i szybko zaburzyć produkcję czerwonych krwinek, płytek oraz prawidłowych białych krwinek. W tym tekście wyjaśniam, jakie objawy powinny wzbudzić czujność, jak wygląda diagnostyka i od czego zależy leczenie. To ważne, bo przy tej chorobie szybka reakcja naprawdę zmienia przebieg dalszych decyzji.
Najważniejsze fakty, które warto uchwycić od razu
- Choroba rozwija się w szpiku i wypiera zdrowe komórki krwi, dlatego daje osłabienie, infekcje i krwawienia.
- Niepokoić powinny: gorączka, nawracające infekcje, siniaki bez urazu, krwawienie z nosa lub dziąseł, bladość i duszność.
- Rozpoznanie opiera się na morfologii, badaniu szpiku, cytometrii przepływowej oraz badaniach genetycznych.
- Leczenie dobiera się do podtypu choroby, wieku, stanu ogólnego i profilu mutacji, a nie według jednego uniwersalnego schematu.
- Niektóre postacie, zwłaszcza promielocytowa, wymagają działania natychmiast, bo wiążą się z dużym ryzykiem krwawień.
Czym jest AML i dlaczego rozwija się tak szybko
W szpiku kostnym powstają wszystkie komórki krwi. Gdy w tym miejscu zaczynają dominować niedojrzałe komórki mieloidalne, czyli blasty, prawidłowa produkcja krwinek zostaje zablokowana. Efekt jest prosty, ale dla organizmu bardzo groźny: spada liczba czerwonych krwinek, płytek i dojrzałych leukocytów, a to oznacza jednocześnie niedokrwistość, skłonność do krwawień i większą podatność na infekcje.
Z mojej perspektywy najważniejsze jest to, że ten proces nie „dojrzewa” powoli przez lata. On potrafi przyspieszyć nagle, dlatego człowiek, który jeszcze niedawno funkcjonował w miarę normalnie, po kilku tygodniach zaczyna czuć wyraźny spadek formy. W klasycznym ujęciu rozpoznanie opiera się zwykle na obecności co najmniej 20% blastów w szpiku lub krwi, choć w części podtypów znaczenie ma też konkretna zmiana genetyczna i wtedy próg bywa niższy.
- Niedokrwistość daje osłabienie, bladość, zadyszkę i męczliwość.
- Małopłytkowość zwiększa ryzyko siniaków, wybroczyn i krwawień.
- Neutropenia sprawia, że infekcje pojawiają się łatwiej i mogą szybciej się nasilać.
To właśnie dlatego ten nowotwór nie jest „tylko chorobą krwi”, ale stanem, który bardzo szybko wpływa na całe ciało. A kiedy mechanizm jest już jasny, najważniejsze staje się wychwycenie pierwszych sygnałów i nieprzeczekiwanie ich bez diagnostyki.
Objawy, których nie warto przeczekać
Jak podaje NCI, pierwsze dolegliwości często rozwijają się w ciągu 4-6 tygodni przed rozpoznaniem. To ważna wskazówka, bo wiele osób przez chwilę zakłada, że chodzi o grypę, przemęczenie albo „spadek odporności”. Problem w tym, że przy ostrej białaczce takie tłumaczenie może kosztować zbyt dużo czasu.
| Objaw | Co może za nim stać | Dlaczego to ważne |
|---|---|---|
| Gorączka, dreszcze, częste infekcje | Spadek prawidłowych białych krwinek | Układ odpornościowy nie działa tak, jak powinien |
| Osłabienie, bladość, duszność przy wysiłku | Niedokrwistość | Tlen jest gorzej transportowany do tkanek |
| Siniaki bez urazu, wybroczyny, krwawienie z nosa lub dziąseł | Małopłytkowość i zaburzenia krzepnięcia | Ryzyko krwawienia rośnie nawet po drobnych urazach |
| Bóle kości, spadek apetytu, utrata masy ciała | Rozrost komórek białaczkowych w szpiku | Objawy są mniej charakterystyczne, ale klinicznie istotne |
| Nagłe splątanie, silny ból głowy, duszność | Bardzo wysoka liczba leukocytów i możliwa leukostaza | To może wymagać pilnej pomocy szpitalnej |
Najczęstszy błąd polega na tym, że ktoś widzi tylko jeden objaw, na przykład osłabienie, i próbuje go wyjaśnić trybem życia. Ja wolę patrzeć na zestaw sygnałów: jeśli osłabieniu towarzyszą infekcje, krwawienia albo wyraźna bladość, nie ma sensu zwlekać. Gdy taki obraz się pojawia, diagnostyka powinna ruszyć od razu, a nie „przy okazji”.
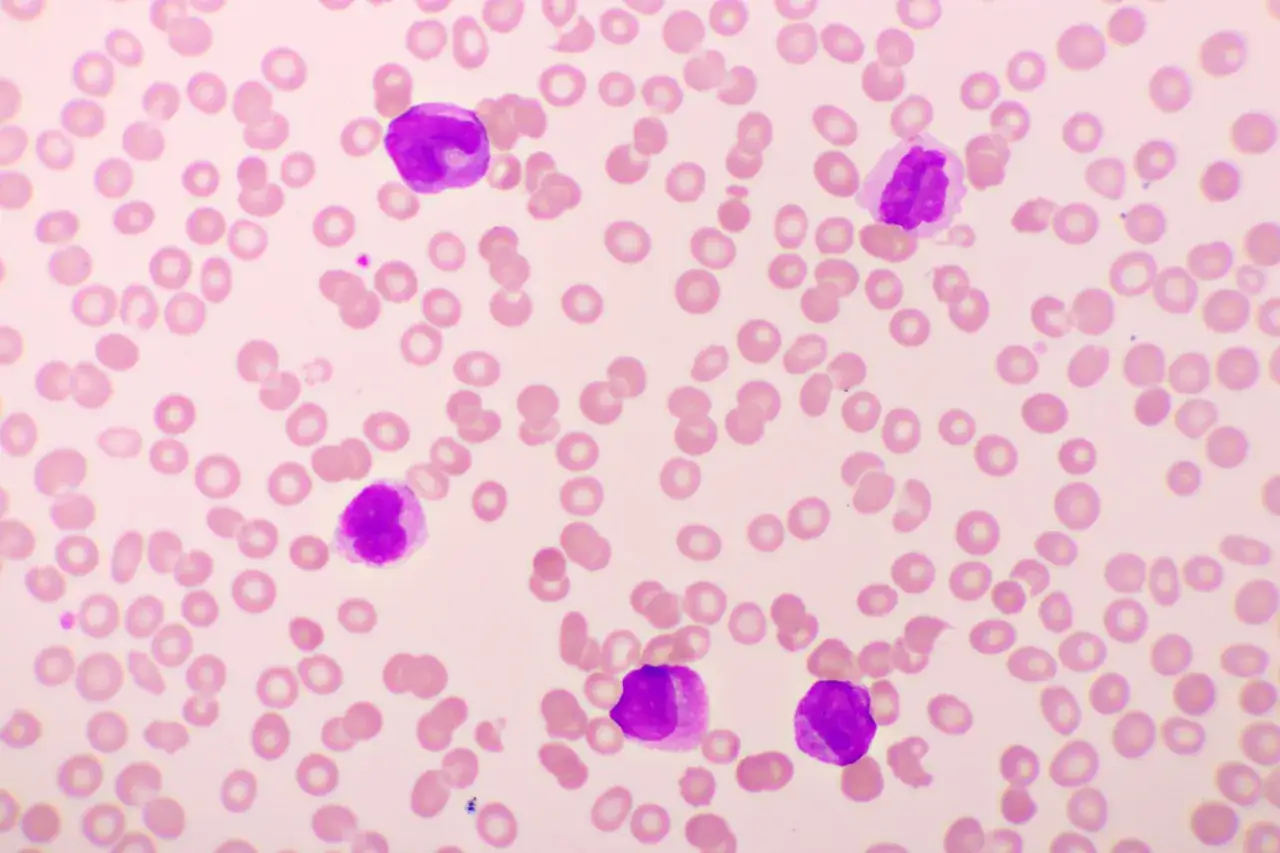
Jak rozpoznaje się chorobę krok po kroku
Tu nie wystarcza jeden wynik z laboratorium. Rozpoznanie opiera się na kilku badaniach, które wzajemnie się uzupełniają i pozwalają nie tylko potwierdzić chorobę, ale też ocenić jej biologiczne zachowanie. W praktyce najpierw wychwyca się problem w morfologii, a potem wchodzi diagnostyka szpiku i genetyki.
| Badanie | Co pokazuje | Po co jest potrzebne |
|---|---|---|
| Morfologia krwi z rozmazem | Niedokrwistość, małopłytkowość, obecność blastów | To zwykle pierwszy sygnał, że coś jest nie tak |
| Aspiracja i biopsja szpiku | Odsetek blastów i obraz komórek w szpiku | Potwierdza lub wyklucza AML |
| Cytometria przepływowa | Immunofenotyp komórek | Pomaga odróżnić AML od innych białaczek |
| Cytogenetyka i FISH | Zmiany chromosomowe | Wpływa na rokowanie i wybór leczenia |
| Badania molekularne | Mutacje, np. FLT3, IDH1, IDH2, NPM1 | Umożliwiają leczenie celowane i precyzyjniejszą kwalifikację ryzyka |
W praktyce ważne jest też tempo. Wyniki genetyczne nie są dodatkiem „na później”, tylko często decydują o tym, jaką terapię zacznie się najpierw. Dlatego współczesna diagnostyka działa równolegle: potwierdza chorobę, a jednocześnie zbiera dane potrzebne do leczenia. W części przypadków to właśnie profil genetyczny przesądza o rozpoznaniu już przy 10-19% blastów, a nie tylko przy klasycznym progu.
Ja patrzę na ten etap jak na wyścig z czasem, ale bez zgadywania. Trzeba działać szybko, tylko że szybko nie znaczy chaotycznie. Kiedy badania są już zebrane, można przejść do najważniejszego pytania: jak leczyć konkretną postać choroby.
Leczenie nie jest jedno i to samo dla wszystkich
Nie ma jednego schematu, który pasuje do każdej osoby z AML. Decyzje zależą od wieku, stanu ogólnego, mutacji, wcześniejszych chorób oraz tego, czy pacjent kwalifikuje się do leczenia intensywnego. W praktyce najczęściej rozważa się kilka ścieżek równolegle, bo nowoczesna hematologia nie opiera się już wyłącznie na samej chemioterapii.
Gdy można zastosować leczenie intensywne
U pacjentów, którzy są w dobrej kondycji ogólnej, celem jest zwykle indukcja remisji, czyli możliwie szybkie wyciszenie choroby. Stosuje się intensywną chemioterapię, a po uzyskaniu odpowiedzi przychodzi etap konsolidacji, który ma zmniejszyć ryzyko nawrotu. W wybranych przypadkach, zwłaszcza przy wyższym ryzyku genetycznym, rozważa się allogeniczny przeszczep komórek krwiotwórczych od dawcy.
Gdy potrzebne jest podejście mniej obciążające
Jeśli wiek lub choroby współistniejące nie pozwalają na agresywne leczenie, sięga się po schematy mniej intensywne. Często łączy się leki hipometylujące, takie jak azacytydyna lub decytabina, z wenetoklaksem, czyli lekiem ukierunkowanym na białko BCL-2. To nie jest „słabsza wersja” leczenia, tylko rozwiązanie dobrane do innego profilu pacjenta.
Przeczytaj również: Przerzuty do kości - Jak rozpoznać objawy i chronić sprawność?
Gdy biologia choroby podpowiada terapię celowaną
W części przypadków znaczenie mają konkretne mutacje. Wtedy lekarz może dołączyć leczenie ukierunkowane na dany mechanizm molekularny, na przykład przy zmianach FLT3 albo IDH1/IDH2. W praktyce zyskujemy dzięki temu więcej niż samą nazwę leku: dostajemy terapię dopasowaną do biologii nowotworu, a nie tylko do jego lokalizacji w szpiku.
W niektórych podtypach, zwłaszcza po przebytym MDS albo po leczeniu przeciwnowotworowym, stosuje się także CPX-351, czyli liposomalne połączenie cytarabiny i daunorubicyny. To pokazuje, jak bardzo spersonalizowane stało się leczenie tej choroby. Z mojej perspektywy najczęstszy błąd polega na myśleniu, że białaczka zawsze oznacza „jedną ciężką chemię” - dziś to już po prostu nie jest prawda.
Leczenie odbywa się zwykle w szpitalu, bo trzeba kontrolować infekcje, krwawienia, spadki morfologii i ryzyko zespołu lizy guza, czyli gwałtownego rozpadu komórek nowotworowych z obciążeniem dla nerek i metabolizmu. Gdy leukocyty są skrajnie wysokie, na przykład powyżej 100 × 109/l, może dojść do leukostazy, a wtedy sytuacja staje się pilna. To właśnie te szczegóły decydują, czy leczenie prowadzi się spokojnie, czy trzeba działać ratunkowo.
W tym miejscu warto wyróżnić jeden podtyp, w którym zwłoka bywa szczególnie groźna.
Dlaczego ostra promielocytowa wymaga natychmiastowej reakcji
Ostra promielocytowa to szczególna postać AML, bo bardzo często wiąże się z ciężkimi zaburzeniami krzepnięcia i ryzykiem groźnych krwawień. Tu nie chodzi wyłącznie o niski poziom płytek. Problem polega też na tym, że organizm zużywa czynniki krzepnięcia w sposób chaotyczny, co może prowadzić do rozsianego wykrzepiania wewnątrznaczyniowego, czyli DIC.
To właśnie w tym podtypie czas ma znaczenie dosłownie z dnia na dzień. Gdy lekarz silnie podejrzewa tę postać choroby, leczenie może zostać rozpoczęte natychmiast, jeszcze zanim spłyną wszystkie wyniki. Standardem u chorych z niskim lub pośrednim ryzykiem jest skojarzenie ATRA, czyli kwasu all-trans-retinowego, z trójtlenkiem arsenu; przy wyższym ryzyku dołącza się też chemioterapię.
- łatwe siniaczenie i wybroczyny powinny od razu zwrócić uwagę,
- krwawienie z nosa lub dziąseł nie jest tu objawem „byle jakim”,
- nagłe pogorszenie stanu ogólnego wymaga pilnej oceny w ośrodku hematologicznym.
To jedna z tych sytuacji, w których szybkie postępowanie naprawdę zmienia rokowanie. Po takim rozpoznaniu następny temat brzmi już nie „czy leczyć”, ale „jak ocenić szanse i jak prowadzić dalszą terapię”.
Co wpływa na rokowanie i powrót do codzienności
Rokowanie w AML nie wynika z jednego parametru. Liczy się wiek, stan ogólny, profil genetyczny choroby, tempo uzyskania remisji i to, czy po leczeniu początkowym pozostają ślady choroby niewidoczne w zwykłych badaniach. Te ślady określa się jako MRD, czyli chorobę resztkową. Negatywny wynik MRD nie daje absolutnej gwarancji, ale zwykle jest dobrym znakiem.
- Wiek i choroby współistniejące wpływają na to, jak intensywnie można leczyć.
- Genetyka nowotworu pomaga odróżnić chorobę bardziej wrażliwą na leczenie od tej o wyższym ryzyku nawrotu.
- Odpowiedź na pierwszą terapię pokazuje, czy wybrany schemat działa zgodnie z oczekiwaniami.
- MRD pomaga ocenić, czy choroba została wygaszona głębiej niż widać w mikroskopie.
- Możliwość przeszczepu bywa kluczowa u części pacjentów z wyższym ryzykiem.
Warto też pamiętać, że remisja nie zawsze oznacza koniec leczenia. Często jest dopiero etapem, po którym zapada decyzja o konsolidacji, obserwacji albo przeszczepie. Dla pacjenta bywa to emocjonalnie trudne, bo po pierwszym „dobrym wyniku” pojawia się kolejny plan, ale medycznie ma to sens: leczenie AML układa się w sekwencję, a nie w pojedynczy zastrzyk nadziei.
Z tych powodów pierwsze tygodnie po diagnozie dobrze traktować jak etap organizowania leczenia, a nie pasywnego czekania. To prowadzi do bardzo praktycznego pytania: co zrobić, żeby nie pogubić się w tym wszystkim.
Jak przejść pierwsze tygodnie po diagnozie bez chaosu
Najbardziej pomaga porządek. Warto od początku mieć zapisane: podtyp choroby, najważniejsze wyniki mutacji, plan leczenia, datę kolejnej kontroli i numer kontaktowy do ośrodka. Jeśli pojawiają się gorączka, krwawienie, nasilona duszność albo nagłe osłabienie, nie czekałbym na „następny wolny termin” - w AML takie objawy trzeba zgłaszać od razu.
- Zapytaj, jaki jest dokładny podtyp choroby i czy leczenie ma być intensywne czy mniej intensywne.
- Ustal, czy wykonano już badania genetyczne i czy trzeba je jeszcze rozszerzyć.
- Dowiedz się, kiedy będzie kontrola morfologii, szpiku i ewentualnej MRD.
- Nie bierz na własną rękę leków ani suplementów, jeśli mogą zwiększać ryzyko krwawień lub wchodzić w interakcje z terapią.
- Ustal, przy jakich objawach masz zgłosić się pilnie do szpitala, a przy jakich wystarczy kontakt telefoniczny z oddziałem.
W tej chorobie naprawdę liczy się nie tylko terapia, ale też szybkie reagowanie na objawy, dobra komunikacja z zespołem i konsekwentne kontrole. To właśnie ten zestaw najczęściej porządkuje pierwsze tygodnie i zmniejsza chaos, który łatwo pojawia się po diagnozie.